 |
 Как обустроить мансарду?  Как создать искусственный водоем?  Как наладить теплоизоляцию?  Как сделать стяжку пола?  Как выбрать теплый пол?  Зачем нужны фасадные системы?  Что может получиться из балкона? |
Главная страница » Энциклопедия строителя
содержание:
[стр.Введение] [стр.1] [стр.2]
страница - 0
Термодинамические функции димерных молекул трихлоридов лантана и лантанидов, Ln2Cl6(r)
Горохов Л.Н. (l.gorokhov@g23.relcom.ru), Осина Е.Л.
Институт теплофизики экстремальных состояний Объединенного института высоких температур РАН, Москва
Введение. Пары галогенидов лантанидов состоят в основном из мономерных молекул LnX3. Наряду с этим, в парах присутствуют в относительно небольших количествах и более сложные комплексы, в первую очередь димерные молекулы Ln2X6. Таким образом, для термодинамического моделирования процессов с участием галогенидов лантанидов необходимы термодинамические данные не только для мономерных, но также и димерных молекул. В настоящей работе изложены результаты выбора молекулярных постоянных и расчета термодинамических функций димерных молекул трихлоридов лантанидов, Ln2Cl6(г). Экспериментальные данные по молекулярным постоянным этих соединений практически отсутствуют. В обзоре М. Харгиттаи [1] приведены неопубликованные экспериментальные и расчетные данные МакКензи и др. (ссылка [422] в работе [1]) по структуре молекул Dy2Cl6. Гиричева и др. [2, 3] исследовали строение Er2Cl6 и Lu2Cl6. Спектры этих молекул не изучены. Недавно опубликованы результаты квантово-механических расчетов Ковача [4] для La2Cl6 и Dy206, полученные методом функционала плотности (DFT) в варианте B3-P86. В работе Капала и др. [5] приведены результаты расчетов методом функционала плотности (вариант B3LYP) для Ce2d6, P^U, Nd2d6 и Dy2d6. В отчете по проекту РФФИ [6] изложены результаты прецизионных ab initio расчетов Соломоника и др. строения и частот колебаний молекул La2Cl6 и Lu2Cl6. Сведения об электронных уровнях димерных молекул трихлоридов лантанидов в литературе отсутствуют. В связи с этим большинство молекулярных постоянных рассматриваемых соединений, необходимых для расчета их термодинамических функций, в настоящей работе оценены. Впервые рассчитаны таблицы термодинамических функций для всего ряда молекул Ln206 в интервале температур 298.15 -3000 К. Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (грант 01-03-32194).
Структура и геометрические параметры. На основании результатов работ [1-6] и в согласии с данными более ранних исследований подобных соединений [7] для димерных молекул трихлоридов лантана и лантанидов Ln206 принята мостиковая структура точечной группы симметрии D2h, в которой концевые атомы хлора Clt лежат в плоскости,
перпендикулярной плоскости кольца Ln-Clb - Ln-Clb (Clb - атом хлора в мостике), с числом симметрии о = 4. (рис. 1).
Произведения моментов инерции IaIbIc вычислены по структурным параметрам, приведенным в табл. 1. Значения концевых межатомных расстояний r(Ln-Cl)t в молекулах Ln206 приняты по экспериментальным данным, приведенным в [1-3], и результатам квантово-химических расчетов [5, 6]. Для остальных димерных молекул эти расстояния оцненены нами по соответствующим величинам для молекул LnCl3, с учтом плавного уменьшения их значений в ряду La2Cl6 - Lu2Cl6 вследствие лантанидного сжатия. Величины r(Ln-Q)b, для которых отсутствуют литературные данные, приняты, исходя из разности r(Ln-С1)ь - r(Ln-Q)t = 0.2 A, полученной в [1-6], а также имеющей достаточно постоянное значение для родственных молекул Al2Cl6 и Ga2Cl6 [7]. Значения углов ZClt-Ln-Clt и ZClb-Ln-Clb приняты по имеющимся литературным данным [1-6] или оценены на основании этих данных. Приняты следующие значения погрешностей оцененных молекулярных
постоянных: r(Ln-Cl)t - 0.02 A, r(Ln-d)b - 0.03 A, ZClt-Ln-Clt и ZClb-Ln-Clb - 5°. В случае
величин, найденных из экспериментальных данных, погрешности взяты из соответствующих
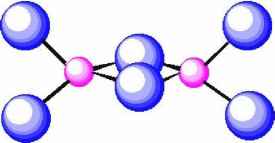
Рис. 1. Структура молекул Ln2d6
работ [1- 3].
Таблица 1. Принятые структурные параметры молекул Ln2Cl6(r) (Ln = La-Lu)
Молекула | r(Ln-Cl)t | r(Ln-Cl)b | ZClt-Ln-Clt | ZClb-Ln-Clb |
A | град | |||
La2Cl6 | 2.58 | 2.81 | 116 | 81 |
Ce2Cl6 | 2.57 | 2.78 | 116.5 | 83 |
Pr2Cl6 | 2.55 | 2.75 | 116 | 83 |
Nd2Cl6 | 2.53 | 2.74 | 116 | 81 |
Pm2Cl6 | 2.53 | 2.73 | 117 | 83 |
Sm2Cl6 | 2.52 | 2.72 | 117 | 83 |
Eu2Cl6 | 2.50 | 2.70 | 117 | 83 |
Gd2Cl6 | 2.47 | 2.67 | 117 | 83 |
Tb2Cl6 | 2.47 | 2.67 | 117 | 84 |
Dy2Cl6 | 2.45 | 2.68 | 117 | 84 |
Ho2Cl6 | 2.45 | 2.65 | 117 | 84 |
Er2Cl6 | 2.44 | 2.65 | 117 | 84 |
Tm2Cl6 | 2.42 | 2.62 | 118 | 84 |
Yb2Cl6 | 2.41 | 2.61 | 118 | 84 |
Lu2Cl6 | 2.37 | 2.59 | 119 | 84 |
Частоты колебаний. Частоты колебаний димерных молекул Ln206 оценены главным образом на основании результатов прецизионных ab initio расчетов Соломоника и др. [6], проведенных для La2Cl6 и Lu2Cl6, с учетом данных квантово-химических расчетов [4, 5], полученных методом DFT. Наличие надежных данных для первого и последнего членов ряда лантанидов удобно в том отношении, что позволяет проводить оценку молекулярных констант остальных молекул с использованием концепции лантанидного сжатия. Следует отметить, что в расчетах Капала и др. [5] для значения частоты неплоского колебания v11 молекул Ce2d6, Рг2С16, Nd2d6 получены величины 12, 10, 12 см-1 соответственно, а для Dy206 - 22см-1. Три первые значения представляются слишком низкими, а последнее -слишком высоким для этой частоты колебания, если сравнивать их с экспериментально
содержание:
[стр.Введение] [стр.1] [стр.2]