 |
 Как обустроить мансарду?  Как создать искусственный водоем?  Как наладить теплоизоляцию?  Как сделать стяжку пола?  Как выбрать теплый пол?  Зачем нужны фасадные системы?  Что может получиться из балкона? |
Главная страница » Энциклопедия строителя
содержание:
[стр.Введение] [стр.1] [стр.2] [стр.3]
страница - 2
раствор KCl. Таким образом, основополагающей величиной является мембранный потенциал ф3. Для идеальной мембраны в отсутствие внешнего тока он является прямой и специфической функцией активности определяемого иона в растворе и описывается электродной функцией Нернста [3-6]. На практике обычно не достигается идеальной селективности электрода. Поэтому рассматривают дополнительные вклады в общую величину активности, которые появляются в результате присутствия мешающих ионов в исследуемом растворе. Полуэмпирическим, но довольно удачным приближением, описывающим поведение мембранных электродов в реальных системах, является уравнение Никольского [2]; однако теоретическое подтверждение его справедливости было получено лишь для отдельных случаев [3].
Применение общей мембранной теории для описания поведения электродов с жидкими мембранами с учетом диссоциации/ассоциации и комплексообразования ионообменника, присутствия конкурирующих ионов, различной валентности у противоионов и т. д. показало, что величина мембранного потенциала (и, в конечном счете, ЭДС ионоселективного электрода) является сложной функцией не только активностей, но и чисел переноса ионов, а также констант устойчивости комплексов и коэффициентов распределения компонентов (или комплексов). Детальный анализ различных случаев приведен в монографии [3].
Характеристики электродов 1-5 в растворах хлорида, нитрата и сульфата кобальта (II) приведены в таблице 2. Как видно из таблицы, ТПЭ с концентрацией CoCl2 0,05 и 0,19 моль-л-1 не проявляют электродноактивных свойств - область линейности у электродов 1 и 5 отсутствует. Для электрода 2 в растворах CoCl2 при pH=3;4 наблюдается широкая линейная область электродной функции - от 10-6 до 10-1 моль-л-1; в растворах Co(NO3)2 область линейности заметно меньше, а в CoSO4 еще меньше. Поведение электрода 3 практически одинаково в растворах CoCl2 (pH=3;4) и Co(NO3)2 (pH=5) -линейная область ограничена интервалом 10-4 - 10-1 моль-л-1, тогда как в растворе CoSO4 области линейности вообще не наблюдалось. Наилучшие характеристики демонстрирует электрод 4, мембрана которого содержит комплексные частицы двух сортов - [Co2Cl3]+ и [Co2Cl4(L)2]0 (табл. 1).
Значение крутизны электродной функции (табл. 2) варьируется в широких пределах и существенно зависит как от концентрации CoCl2 в электродноактивной мембране, так и от величины pH и природы аниона в исследуемом растворе. При этом в растворах CoSO4, где анион двухвалентный, крутизна электродной функции принимает много меньшие значения, чем в растворах CoCl2 и Co(NO3)2. Во всех случаях электродная функция в интервале линейности имеет анионный характер.
Таблица 2. Электродные характеристики Со-СЭ акрилонитрила и бутадиена и CoCl2
на
основе сополимера
№ электрода | Анализируемый раствор | pH | Характеристики электродной функции | |
Область линейности, моль-л-1 | Крутизна, мВ/рСсо | |||
1 | CoCl2 | 5 | Область линейности отсутствует | - |
2 | CoCl2 | 3 4 | 1х10"6 - 1х10-1 1х10"6 - 1х10-1 | 23±1 22±1 |
Co(NO3)2 | 4 | 1х10"4 - 1х10-1 | 54±1 | |
CoSO4 | 5 | 1х10"4 - 1х10"2 | 7,5±1,0 | |
3 | CoCl2 | 3 4 | 1х10"4 - 1х10-1 1х10"4 - 1х10-1 | 26±1 25±1 |
Co(NO3)2 | 5 | 1х10"4 - 1х10-1 | 31±1 | |
CoSO4 | 4 | Область линейности отсутствует | - | |
4 | CoCl2 | 3 4 | 1х10"6 - 1х10-1 1х10"6 - 1х10-1 | 33±1 35±1 |
Co(NO3)2 | 5 | 1х10"5 - 1х10-1 | 30±1 | |
CoSO4 | 4,5 | 1х10"4 - 1х10-1 | 8,5±1,0 | |
5 | CoCl2 | 5 | Область линейности отсутствует | - |
Электродные функции для ИСЭ с мембраной оптимального состава (электрод 4) в разных растворах представлены на рис. 3; влияние pH на ЭДС в растворе CoCl2 - на рис. 4.
Проанализируем полученные результаты. Четко выраженная субнернстовская функция является типичной для ИСЭ с жидкими мембранами [4], аналогом которых является исследуемый электродный материал - ТПЭ. Поскольку отклонение от нернстовской зависимости воспроизводимо, такие электроды можно использовать для аналитических целей [6]. Как видно из таблицы 2 и рис. 3, наблюдается корреляция между электродными характеристиками ИСЭ с мембраной на основе ТПЭ, содержащего CoCl2, и способностью аниона в анализируемом растворе к комплексообразованию: Cl- > NO3- > SO42-. Это свидетельствует о том, что мембранный потенциал электрода, как и следовало ожидать, определяется процессами комплексообразования. Подробное объяснение потенциалобразующих процессов выходит за рамки данной работы.
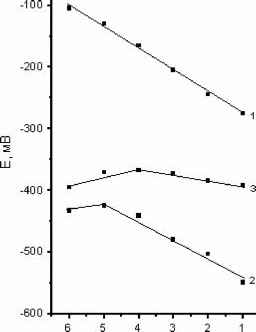
Рис. 3. Электродные функции электрода 4
в растворах: 1 - CoCl2, рН=4; 2 - Co(NO3)2,
рН=5; 3 - CoSO4, рН=4,5.
рСо
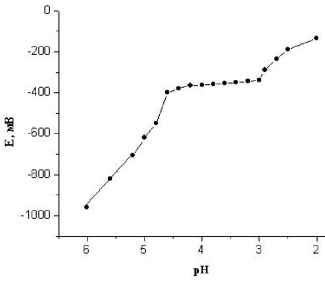
Рис. 4. Зависимость потенциала электрода 4 от рН анализируемого
"3"1
раствора. 0^^=1x10" моль-л .
Для жидких мембран на основе нейтральных переносчиков (родственных исследуемым материалам) достаточно часто наблюдаются значительные отклонения от идеальности электродной функции, обусловленные анионными эффектами. Теоретический анализ показывает, что в результате этого влияния для катионных комплексов можно получить анионную функцию [3]; возможна и обратная ситуация. На практике анионный характер электродной функции катион"селективных электродов нередко встречается не только у жидких, но и у твердых мембран в случае электродов,
содержание:
[стр.Введение] [стр.1] [стр.2] [стр.3]